Método de desinfección para el establecimiento in vitro de bulbos de ajo (Allium sativum L.)
Contenido principal del artículo
Resumen
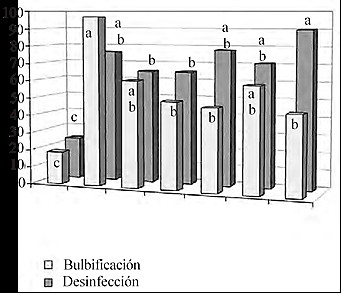
Los ápices de crecimiento de los bulbos de ajo (dientes), son explantes vigorosos para los trabajos de cultivo de tejidos, pero usualmente presentan altos niveles de contaminación con los microorganismos del suelo, por ser órganos de crecimiento subterráneo. Los experimentos están dirigidos a comparar diferentes variantes para la desinfección del bulbo, utilizando como desinfectantes hipoclorito de sodio al 0.5-5% y bicloruro de mercurio al 0.1 %. Durante el desarrollo de los explantes, se contabilizaron las plantas contaminadas y las plantas vivas, para evaluar la supervivencia de los cultivos. El desarrollo de las vitroplantas se evaluó cada 15 días, cuantificando las hojas, las raíces, y las plantas que formaron bulbillos. El procedimiento consistente en aplicar hipoclorito de sodio al 5 % durante 15 minutos; seguido de cortar 1mm de la capa más externa y flamear ligeramente la base del diente permitió obtener niveles de desinfección aceptables de los bulbos de ajo, con valores de descontaminación en el entorno del 70 %, sin producir deterioro de las plantas.
Detalles del artículo

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial 4.0.
Aquellos autores/as que tengan publicaciones con esta revista, aceptan los términos siguientes de la Licencia CC Reconocimiento-NoComercial 4.0 Internacional (CC BY-NC 4.0):
Usted es libre de:
- Compartir — copiar y redistribuir el material en cualquier medio o formato
- Adaptar — remezclar, transformar y crear a partir del material
El licenciador no puede revocar estas libertades mientras cumpla con los términos de la licencia.
Bajo las condiciones siguientes:
- Reconocimiento — Debe reconocer adecuadamente la autoría, proporcionar un enlace a la licencia e indicar si se han realizado cambios. Puede hacerlo de cualquier manera razonable, pero no de una manera que sugiera que tiene el apoyo del licenciador o lo recibe por el uso que hace.
- NoComercial — No puede utilizar el material para una finalidad comercial.
- No hay restricciones adicionales — No puede aplicar términos legales o medidas tecnológicas que legalmente restrinjan realizar aquello que la licencia permite.
La revista no se responsabiliza con las opiniones y conceptos emitidos en los trabajos, son de exclusiva responsabilidad de los autores. El Editor, con la asistencia del Comité de Editorial, se reserva el derecho de sugerir o solicitar modificaciones aconsejables o necesarias. Son aceptados para publicar trabajos científico originales, resultados de investigaciones de interés que no hayan sido publicados ni enviados a otra revista para ese mismo fin.
La mención de marcas comerciales de equipos, instrumentos o materiales específicos obedece a propósitos de identificación, no existiendo ningún compromiso promocional con relación a los mismos, ni por los autores ni por el editor.
Cómo citar
Referencias
Bekheet, S.A. A synthetic seed method through encapsulation of in vitro proliferated bulblets of garlic (Allium sativum L.). Arab J. Biotech. 2006, Vol. 9 (3): 415-426.
Burba, J.L. Los grupos varietales del ajo (Allium sativum L.). Contribución para su entendimiento. Horticultura Argentina. 2008, 27(62): 20-27.
ECP/GR Working group on Allium. 2006. Progress report for the period 2003-2006.http://www.ecpgr.cgiar.org/SteeringCommittee/SC10/StandRep/Allium_standrep.pdf: 21 de septiembre del 2009.
Keller, J. y D.E. Lesemann. 1997. Application of in vitro culture to onion and garlic for the management and use of genetic resources at Gatersleben. Proc.I Symp. Edible Alliaceae SecIL: Burba and C.R. Galmarini Acta Hort. 433.ISHS 1997.
Kim, H.H.; Lee J. K.; Hwang, H.S. and F. Engelmann. 2007. Cryopreservation of garlic germplasm collections using the droplet-vitrification technique. CryoLetters 28 (6), 471-482.
Hassan, N. A.; A. A. El-Halwagi; A. Gaber; M. Al-Awady y A. Khalaf. 2007. Slow growth in vitro conservation of garlic cultivars grow in Egypt: chemical characterization and molecular evaluation. 2007. Global Journal of Molecular Sciences. 2 (2): 67-75.
Izquierdo, H.; Disotuar, R.; Qiñonez Y.; y Bejerano, J. M. 1998. Efectividad de diferentes agentes químicos en la desinfeccion de Allium sativum L. para su implantacion in vitro Taller Internacional «Geminivirus en el Caribe», La Habana, Cuba.
Makowska, Z. J. Keller y F. Engelmann.1999. Cryopreservation of apices isolated from garlic (Allium sativum L.) bulbils and cloves. Cryo-Letters 20: 175- 182.
Muñoz, L.; L. Almaguel; M. Benítez; G. Brito; I. Cáceres; J. J. Castellanos; S. Fraga; J. F. Gil; M. López; A. Prats. 2010. El cultivo y mejoramiento de la producción de ajo en Cuba. Agricultura Organica. 1: 18-21.
Murashige, T.; F. Skoog,. 1962. A revised meduim for rapid growth and bioessays with tobacco tissue cultures. Physiol. Plant. 15: 473-497.
Neveen A. H.; A. A. El-Halwagi, A. Gaber, M. El-Awady y A. 2007. Khalaf. Slow-Growth in vitro conservation of garlic cultivars grow in Egypt. Global Journal of Molecular Sciences 2 (2): 67-75.
Seif El-Nasr H. GadEl-Hak; , A. Z. Kasem ; M.M.M. Yasser y E. S. Asmaa. 2011. Growth and cytogenetical properties of micro-propagated and successfully acclimatized garlic (Allium sativum L.) clones with a modified shoot tip culture protocol. Journal of Horticultural Science & Ornamental Plants 3 (2): 115-129.
Shemesh, E; O.Scholten, H. D. Rabinowitch y R. Kamenetsky.2008. Unlocking variability: inherent variation and developmental traits of garlic plants originated from sexual reproduction. Planta.227(5):1013- 1024.
Stavìlíková, H. 2008. Morphologycal characteristics of garlic (Allium sativum L.) genetic resources collection- Information. Hort. Sci. (Prague) 35 (3): 130-135.
Torres M. A.; M. R. López, A. J. Rodríguez y M. Benítez. 2008. Conservación de germoplasma de ajo (Allium sativum L.) por reducción de la tasa de crecimiento. Agrotecnia de Cuba. 32 (2):46-55.