Caracterización morfo-agronómica de sandía (Citrullus lanatus (Thunb.) Matsum. et Nakai) en la localidad de cabezada, provincia Granma, Cuba
Contenido principal del artículo
Resumen
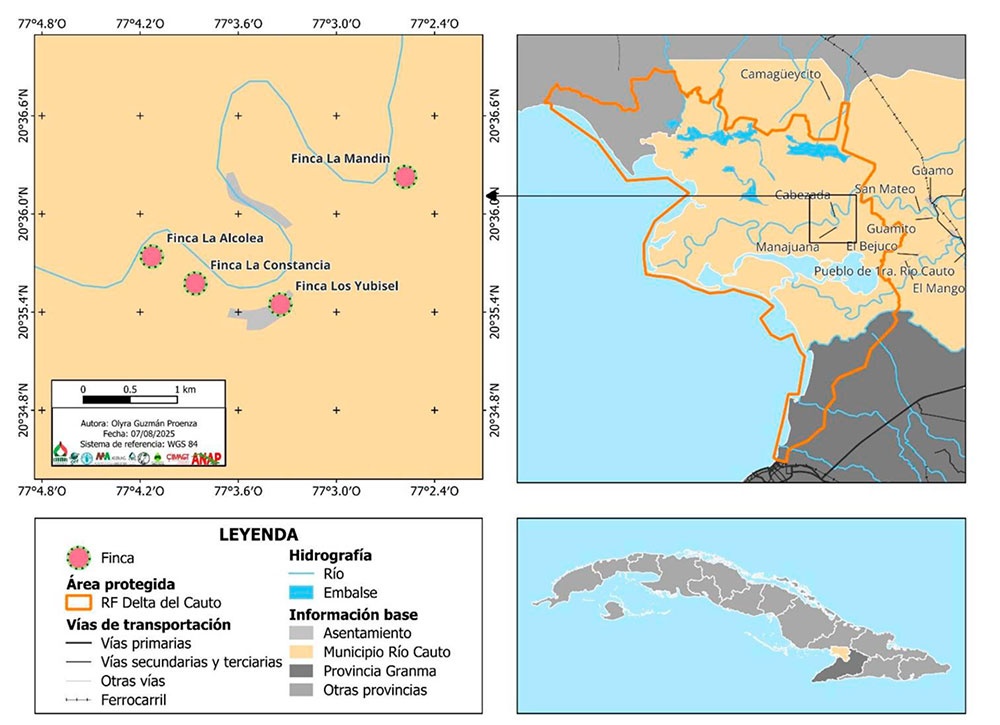
En Cuba existen 12 cultivares comerciales de sandía (Citrullus lanatus), pero los germoplasmas locales han sido menos estudiados en la literatura científica, factor que acelera su erosión genética. El proyecto "Introducción de nuevos métodos agrícolas para la conservación y el uso sostenible de la biodiversidad" busca conservar este cultivo en la comunidad de Cabezada, del Refugio de Fauna Delta del Cauto, provincia de Granma, donde se había identificado el cultivar local 'Patisito'. Esta investigación caracterizó morfo-agronómicamente el germoplasma local para verificar su existencia. La metodología incluyó: 1) adquisición de germoplasma mediante encuestas y colecta de semillas en cuatro fincas de la Cooperativa Ramón Ramos (en la localidad de Cabezada) y 2) caracterización morfológica del germoplasma obtenido con descriptores mínimos de Cucurbitaceae, análisis estadísticos y coeficiente de correlación de Pearson. El experimento se estableció en la finca "Villegas" (Güira de Melena, Artemisa) con siembras escalonadas para evitar polinización cruzada. Los resultados determinaron que el germoplasma adquirido no corresponde al cultivar 'Patisito' descrito por los agricultores locales, mostrando heterogeneidad en caracteres clave para su identificación. Sin embargo, presentó homogeneidad en cinco caracteres: hábito de crecimiento rastrero, lobulación foliar débil, ausencia de flores hermafroditas, corteza verde claro y pulpa rosada. La correlación positiva entre frutos más pesados y semillas más largas sugiere una población menos seleccionada para pulpa. La pulpa rosada homogénea indica alta acumulación de licopeno, posible adaptación a la salinidad del Delta del Cauto. Estos hallazgos revelan riesgo de erosión genética y destacan la relevancia de la conservación in situ de este recurso fitogenético adaptado localmente.
Detalles del artículo

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial 4.0.
Aquellos autores/as que tengan publicaciones con esta revista, aceptan los términos siguientes de la Licencia CC Reconocimiento-NoComercial 4.0 Internacional (CC BY-NC 4.0):
Usted es libre de:
- Compartir — copiar y redistribuir el material en cualquier medio o formato
- Adaptar — remezclar, transformar y crear a partir del material
El licenciador no puede revocar estas libertades mientras cumpla con los términos de la licencia.
Bajo las condiciones siguientes:
- Reconocimiento — Debe reconocer adecuadamente la autoría, proporcionar un enlace a la licencia e indicar si se han realizado cambios. Puede hacerlo de cualquier manera razonable, pero no de una manera que sugiera que tiene el apoyo del licenciador o lo recibe por el uso que hace.
- NoComercial — No puede utilizar el material para una finalidad comercial.
- No hay restricciones adicionales — No puede aplicar términos legales o medidas tecnológicas que legalmente restrinjan realizar aquello que la licencia permite.
La revista no se responsabiliza con las opiniones y conceptos emitidos en los trabajos, son de exclusiva responsabilidad de los autores. El Editor, con la asistencia del Comité de Editorial, se reserva el derecho de sugerir o solicitar modificaciones aconsejables o necesarias. Son aceptados para publicar trabajos científico originales, resultados de investigaciones de interés que no hayan sido publicados ni enviados a otra revista para ese mismo fin.
La mención de marcas comerciales de equipos, instrumentos o materiales específicos obedece a propósitos de identificación, no existiendo ningún compromiso promocional con relación a los mismos, ni por los autores ni por el editor.
Cómo citar
Referencias
Aguado, E., García, A., Iglesias-Moya, J., Romero, J., Wehner, T. C., Gómez-Guillamón, M. L., Picó, B., Garcés-Claver, A., Martínez, C., y Jamilena, M. (2020). Mapping a partial andromonoecy locus in Citrullus lanatus using BSA-seq and GWAS approaches. Frontiers in Plant Science, 11, 1243. Disponible en: https://www.frontiersin.org/journals/plant-science/articles/10.3389/fpls.2020.01243/full
Begué-Quiala, G., Planas, J. R. I., Rivera, D. G., Elías, O. C., Trejo, H. M. P., y Rodríguez, D. A. (2022). Cultivo y conservación de frijol por campesinos dispersos en la Reserva de Biosfera Cuchillas del Toa, evidencias del cambio climático. Agrotecnia de Cuba, 46(1), 12-22. Disponible en: https://www.agrotecnia.edicionescervantes.com/index.php/agrotecnia/article/view/40
Brickell, C. D., Alexander, C., Cubey, J. J., David, J. C., Hoffman, M. H. A., Leslie, A. C., Malécot, V., y Jin, X. (2016). International Code of Nomenclature for Cultivated Plants (9th ed.). International Society for Horticultural Science. Disponible en: https://www.ishs.org/sites/default/files/static/ScriptaHorticulturae_18.pdf
Choudhary, H., Padmanabha, K., Jat, G. S., y Behera, T. K. (2023). Challenges of traditional breeding in watermelon. En S. Kr. Dutta, P. Nimmakayala, y U. K. Reddy (Eds.), The Watermelon Genome, 85-130. Springer International Publishing. https://doi.org/10.1007/978-3-031-34716-0_7
Di Rienzo, J. A., Casanoves, F., y Balzarini, M. G. (2008). InfoStat (Versión 2008) [Software]. Grupo InfoStat, Universidad Nacional de Córdoba. Disponible en: http://www.infostat.com.ar
European Cooperative Programme for Plant Genetic Resources (ECPGR). (2008). Minimum descriptor lists for Cucurbita spp., Cucumber, Melon, Watermelon. Disponible en: https://www.ecpgr.org/working-groups/cucurbits/cucurbits-working-group-documents-and-publications-of-interest
Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO). (2014). Normas para bancos de germoplasma de recursos fitogenéticos para la alimentación y la agricultura (Edición revisada). Disponible en: https://www.fao.org/4/i3704s/i3704s.pdf
FAO. (2023). Guía práctica para la aplicación de las normas para bancos de germoplasma de recursos fitogenéticos para la alimentación y la agricultura: Conservación de semillas ortodoxas en bancos de germoplasma de semillas. Comisión de Recursos Genéticos para la Alimentación y la Agricultura, Roma, Italia. FAO. https://doi.org/10.4060/cc0021es
Gao, B., Sun, D., Yuan, G., An, G., Li, W., Liu, J., y Zhu, Y. (2022). Identification of salt tolerance of 121 watermelon (Citrullus lanatus L.) germplasm resources. Journal of Fruit Science, 39(9), 1597-1606. Disponible en: https://www.cabidigitallibrary.org/doi/full/10.5555/20220431670
Gong, C., Zhao, S., Yang, D., Lu, X., Anees, M., He, N., Zhu, H., Zhao, Y., y Liu, W. (2022). Genome-wide association analysis provides molecular insights into natural variation in watermelon seed size. Horticulture Research, 9, uhab074. https://doi.org/10.1093/hr/uhab074
González, D., Sánchez, Y., y Fernández, M. (2014). Análisis hidroquímico con fines de riego de aguas subterráneas de la provincia de Granma. Minería y Geología, 30(4), 38-54. Disponible en: http://www.redciencia.cu/geobiblio/paper/2015-Sanchez-GEO13-O7.pdf
Grumet, R., McCreight, J. D., McGregor, C., Weng, Y., Mazourek, M., Kathleen, R., Labate, J., Davis, A., y Fei, Z. (2021). Genetic resources and vulnerabilities of major Cucurbit crops. Genes, 12(8). https://doi.org/10.3390/genes12081222
Grupo Semillas. (2018). Producción y conservación de semillas nativas y criollas de buena calidad y sanidad. HEKSEPER Colombia. Disponible en: https://www.semillas.org.co/apc-aa-files/5d99b14191c59782eab3da99d8f95126/cartilla-produccion-de-semillas_web.pdf
Guo, S., Zhang, J., Sun, H., Salse, J., Lucas, W. J., Zhang, H., Zheng, Y., Mao, L., Ren, Y., y Wang, Z. (2013). The draft genome of watermelon (Citrullus lanatus) and resequencing of 20 diverse accessions. Nature genetics, 45(1), 51-58. Disponible en: https://www.nature.com/articles/ng.2470
Hailu, B., y Mehari, H. (2021). Impacts of soil salinity/sodicity on soil-water relations and plant growth in dry land areas: A review. J. Nat. Sci. Res, 12(3), 1-10. Disponible en: https://pdfs.semanticscholar.org/c5b7/9e53589f60bc564e2ff61a3c9b8ab309bab7.pdf
Jin, C., Ji, J., Zhao, Q., Ma, R., Guan, C., y Wang, G. (2015). Characterization of lycopene β-cyclase gene from Lycium chinense conferring salt tolerance by increasing carotenoids synthesis and oxidative stress resistance in tobacco. Molecular Breeding, 35(12), 228. https://doi.org/10.1007/s11032-015-0418-y
Kang, B., Zhao, W., Hou, Y., y Tian, P. (2010). Expression of carotenogenic genes during the development and ripening of watermelon fruit. Scientia Horticulturae, 124(3), 368-375. https://doi.org/10.1016/j.scienta.2010.01.027
Khoury, C. K., Brush, S., Costich, D. E., Curry, H. A., de Haan, S., Engels, J. M. M., Guarino, L., Hoban, S., Mercer, K. L., Miller, A. J., Nabhan, G. P., Perales, H. R., Richards, C., Riggins, C., y Thormann, I. (2022). Crop genetic erosion: Understanding and responding to loss of crop diversity. New Phytologist, 233(1), 84-118. https://doi.org/10.1111/nph.17733
Li, N., Shang, J., Wang, J., Zhou, D., Li, N., y Ma, S. (2020). Discovery of the genomic region and candidate genes of the scarlet red flesh color (Yscr) locus in watermelon (Citrullus Lanatus L.). Frontiers in Plant Science, 11. https://doi.org/10.3389/fpls.2020.00116
Mashilo, J., Shimelis, H., Maja, D., y Ngwepe, R. M. (2022). Retrospective genetic analysis of qualitative and quantitative traits in sweet watermelon (Citrullus lanatus var. lanatus): A review. Agronomy, 12(7), 1633. https://doi.org/10.3390/agronomy12071633
Ministerio de la Agricultura de la República de Cuba (MINAG). (2024). Lista Oficial de Variedades Comerciales 2024-2025.
Pearson, K. (1895). Note on regression and inheritance in the case of two parents. Proceedings of the Royal Society of London, 58, 240-242. Disponible en: https://www.jstor.org/stable/115794
Pérez, N., y Caballero, R. (2021). Agroecología en Cuba-Iniciativas y evidencias innovadoras escalables. FAO, MINAG y ACTAF. https://doi.org/10.4060/cb6166es
Prothro, J., Abdel-Haleem, H., Bachlava, E., White, V., Knapp, S., y McGregor, C. (2013). Quantitative trait loci Açassociated with sex expression in an inter-subspecific watermelon population. Journal of the American Society for Horticultural Science, 138(2), 125-130. https://doi.org/10.21273/JASHS.138.2.125
Torres, M., Socorro, A., y Rodríguez, M. I. (2024). Características de la capa superior de los suelos en fincas del Delta del Cauto. Agrotecnia de Cuba 48. https://cu-id.com/2120/v48e18. https://agrotecnia.edicionescervantes.com/index.php/agrotecnia/article/view/799
Wei, C., Chen, X., Wang, Z., Liu, Q., Li, H., Zhang, Y., Ma, J., Yang, J., y Zhang, X. (2017). Genetic mapping of the LOBED LEAF 1 (ClLL1) gene to a 127.6-kb region in watermelon (Citrullus lanatus L.). PLOS ONE, 12(7), e0180741. https://doi.org/10.1371/journal.pone.0180741
Zhang, J., Sun, H., Guo, S., Ren, Y., Li, M., Wang, J., Zhang, H., Gong, G., y Xu, Y. (2020). Decreased protein abundance of lycopene β-Cyclase contributes to red flesh in domesticated watermelon. Plant Physiology, 183(3), 1171-1183. https://doi.org/10.1104/pp.19.01409